Emidio Scarpellini, Valentina Maurizi, Emiliano Lattanzi, Guido Collina, Alessandra Filosa, Carlo Rasetti, Pierangelo Santori
Scenario clinico
Un agricoltore di 60 anni lamenta da circa 3 settimane astenia marcata, febbricola serotina e sudorazione notturna in assenza di tosse, dispnea, disuria, alterazione dell’alvo o altra sintomatologia d’organo; riferisce inoltre calo ponderale di circa 10 kg in 2 mesi.
L’anamnesi patologica remota è significativa solo per una fibrillazione atriale parossistica e il paziente non assume terapia cronica.
A domicilio è stata praticata terapia antibiotica empirica con claritromicina, senza beneficio ed eseguita una ecografia addome, con riscontro di una splenomegalia e multiple linfoadenomegalie addominali.
Obiettivamente il paziente appare defedato, sono presenti piccole linfoadenomegalie a livello laterocervicale di consistenza teso-elastica e una splenomegalia, con milza palpabile a 2 cm dall’arcata costale.
Agli esami ematochimici emerge una pancitopenia con anemia normocitica moderata (Hb 10,1 g/dl), piastrinopenia lieve (118.000/mmc piastrine) e leucopenia lieve (leucociti 3.300/mmc, con formula leucocitaria conservata, ad eccezione dell’assenza di eosinofili), associata ad incremento degli indici biologici di flogosi: PCR 5,3 mg/dl (v.n. <0,5) con procalcitonina lievemente al di sopra dei limiti di norma (0,65 ng/ml con v.n.<0,5). Si segnalano inoltre lieve iperbilirubinemia diretta (0,57 mg/dl) e lieve prolungamento del tempo di protrombina (PT 36,5 sec).
Il quadro clinico è dunque quello di una febbre intermittente da 3 settimane con flogosi sistemica, calo ponderale, linfoadenomegalie diffuse e splenomegalia associata ad una pancitopenia, non responsive a terapia antibiotica empirica con claritromicina.
Ipotesi e iter diagnostico
Le ipotesi diagnostiche che vengono formulate sono le seguenti:
- Patologia infettiva: virale (CMV, EBV, HBV, HCV, HIV), batterica (brucellosi, endocardite subacuta), micobatterica, parassitaria, fungina;
- Patologia neoplastica ematologica: linfoma, leucemia, mieloma multiplo, sindrome mieloproliferativa;
- Patologia immunologica: lupus eritematoso sistemico, sindrome di Felty, sindrome da attivazione macrofagica secondaria ad infezione, sarcoidosi;
- Malattia da deposito: amiloidosi.
La sierologia virale risulta negativa, così come le emocolture. Un ecocardiogramma non mostra vegetazioni endocarditiche. Il quadro clinico viene approfondito mediante TC total body con m.d.c.: a livello del torace si repertano solo addensamenti disatelettasici basali e si conferma la presenza di noduli polmonari e linfoadenomegalie di circa 2 cm, noti in anamnesi. A livello addominale si conferma la splenomegalia (diametro 17 cm) e si documenta la presenza di multiple linfoadenomegalie all’ilo epatico, peri-pancreatiche, para-aortiche, inter-aorto-cavali e inguinali (diametro massimo 2,3 cm) oltre a un nodulo di 1,4 cm surrenalico sinistro; nei limiti la TC cerebrale e del collo.
Durante la degenza si prescrive una terapia antibiotica empirica con levofloxacina e corticosteroidea endovenosa (metilprednisolone20 mg/die), con defervescenza febbrile, normalizzazione della leucoco- e e delle piastrinopenia e riduzione degli indici di flogosi.
Pervengono nel frattempo ulteriori esami ematici: la ricerca degli anticorpi antinucleo è negativa, all’elettroforesi sieroproteica emerge un’importante ipergammaglobulinemia policlonale (Figura 1).
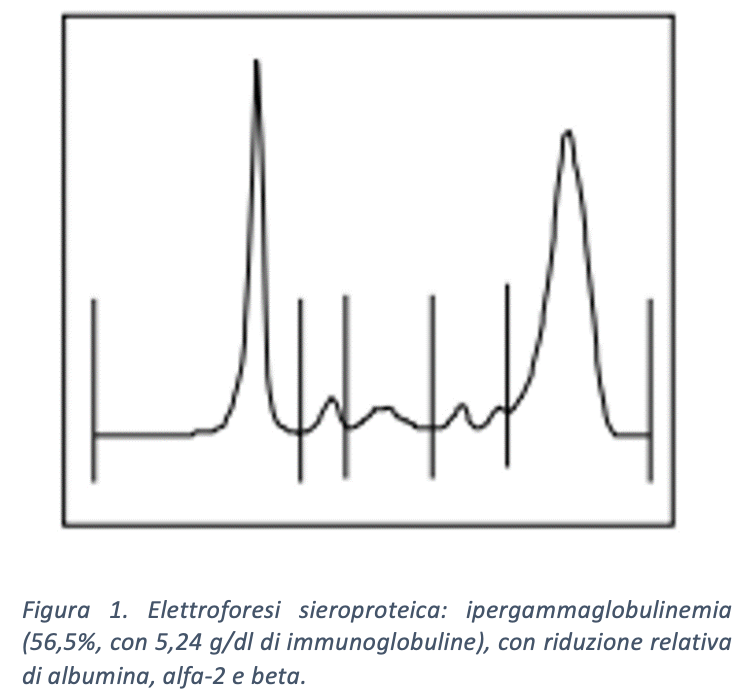
Risultano aumentate anche le catene leggere libere sieriche e urinarie sia kappa che lambda (con rapporto conservato) e la beta2-microglobulina.
Le radiografie dello scheletro in toto non mostrano lesioni osteolitiche né sono presenti ipercalcemia o insufficienza renale. A questo punto è fondamentale uno studio del midollo osseo: alla B.O.M. il quadro è quello di una mielopoiesi iperplastica con plasmocitosi diffusa (10%) verosimilmente reattiva, in assenza di localizzazione linfomatosa. Lo studio immunofenotipico non risulta dirimente.
A completamento, per escludere focolai infettivi o lesioni eteroplastiche misconosciute, si effettua una P.E.T., che documenta iperfissazione a carico delle note linfoadenomegalie, della milza e a livello osteomidollare.
Tutto orienta verso una patologia linfoproliferativa, per cui si esegue una biopsia linfonodale a livello della stazione inguinale e si dimette il paziente in attesa del referto dell’esame istologico con una terapia corticosteroidea per os, in discrete condizioni generali, apiretico.
La sorpresa
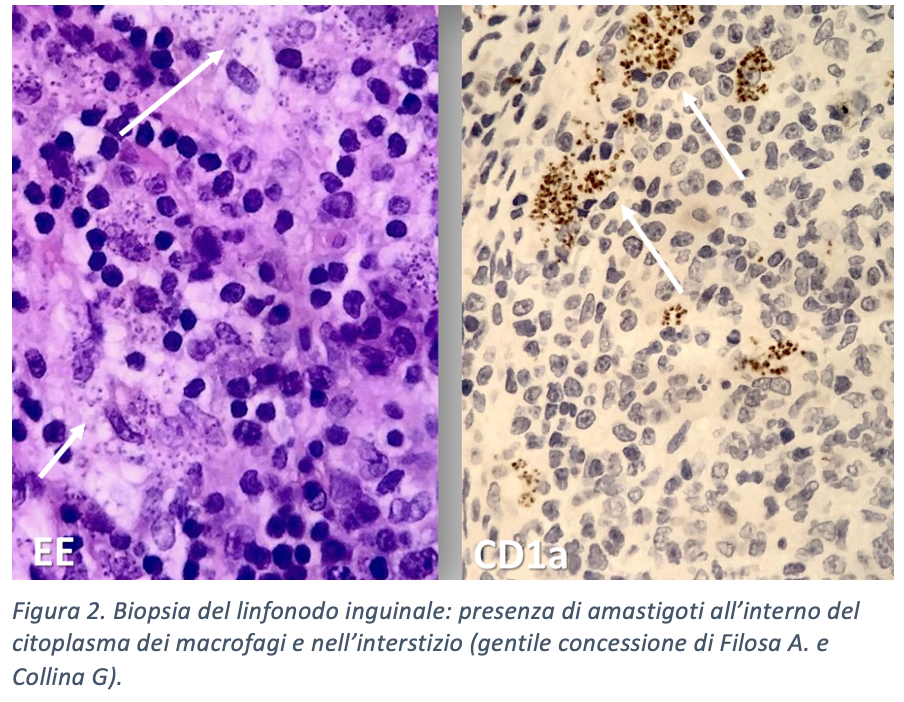
L’esame istologico del linfonodo inguinale mostra una linfoadenite reattiva con presenza nel centro germinativo di clusters di macrofagi con citoplasma ripieno di corpuscoli risultati positivi all' immunocolorazione con anticorpo anti CD1a, riferibili ad amastigoti. Il quadro è quello di una linfadenite reattiva ad eziologia molto probabilmente infettiva, da Leishmania (Figura 2).
Vengono quindi ricercati gli anticorpi anti-Leishmania, che risultano positivi (29,5 UE, con limite 11), e viene fatta diagnosi di Leishmaniosi viscerale.
La Leishmaniosi
La Leishmaniosi è causata da venti specie diverse di protozoi del genere Leishmania ed è trasmessa dalle punture di moscerini flebotomi. Si stima che ogni anno si verifichino in tutto il mondo fra 700.000-1.000.000 nuovi casi e circa 26.000-65.000 decessi. La Leishmaniosi colpisce molti paesi nelle regioni tropicali e subtropicali dell’Africa, dell’America centrale e del Sud America, dell’Asia e della regione del Mediterraneo, è endemica in alcune regioni italiane, tra cui le Marche. In tutta l’area mediterranea la malattia è riemergente, con un aumento dei casi nel corso di tutto il decennio ’90. In Italia, secondo dati dell’Istituto superiore di sanità, l’incidenza annuale a inizio degli anni 2000 è di circa 200 casi, anche se molte regioni soffrono di sotto-notifica.
L’infezione può essere asintomatica, interessare cute e/o mucose (Leishmaniosi cutanea e mucocutanea, rispettivamente) o dare un coinvolgimento sistemico (Leishmaniosi viscerale).
La Leishmaniosi viscerale è causata in particolare da 2 specie di Leishmania: L. Infantum (diffusa nell’area del Mediterraneo e del Medioriente) e L. Donovani (diffusa in Africa e Asia del sud). Nel primo caso il reservoir è costituito essenzialmente dal cane domestico, configurando pertanto una zoonosi, mentre nel secondo caso è riportata anche la trasmissione da uomo a uomo (che costituisce l’unico serbatoio in India).
In rari casi la trasmissione avviene per via parenterale, ad esempio mediante utilizzo di siringhe infette, trasfusioni, trapianti.
Quando sospettarla?
In un paziente che proviene da un’area endemica, un quadro clinico suggestivo è costituito da febbre, calo ponderale, splenomegalia, pancitopenia, eosinofilopenia, aumento degli indici di citonecrosi epatica, iper-gammaglobulinemia e possibile epatomegalia. L’andamento clinico è tendenzialmente subacuto o cronico, raramente acuto. Nei pazienti immunocompromessi possiamo riscontrare manifestazioni atipiche, con coinvolgimento polmonare, pleurico, gastro-intestinale.
Come fare diagnosi?
In un paziente con sospetta Leishmaniosi viscerale, per massimizzare la probabilità di una corretta diagnosi, è indicato utilizzare contemporaneamente differenti approcci diagnostici e differenti campioni, tenendo in considerazione la clinica del paziente, l’origine geografica, la metodica impiegata e l’affidabilità del laboratorio. Gli strumenti che abbiamo a disposizione sono:
-Esame istologico: fondamentale è la visualizzazione dei caratteristici amastigoti nello striscio e/o nella biopsia, che in prima istanza dovrebbe essere effettuata su midollo (gravato, però, da bassa sensibilità: 52-85%), in seconda istanza in linfonodi (sensibilità 52-58%), fegato, buffy coat, o altri siti, in base alla clinica. La biopsia splenica, sebbene abbia un’elevata sensibilità (93-99%), non è raccomandata per l’elevato rischio emorragico.;
-Isolamento del parassita mediante esame colturale;
-Ricerca del DNA del parassita mediante PCR;
-Test sierologico: da solo non è raccomandato per la diagnosi, ma può essere d’aiuto in pazienti con sospetta Leishmanosi viscerale in cui gli altri test diagnostici non possono essere eseguiti o sono negativi. Può essere falsamente negativo nei pazienti immunocompromessi.
Trattamento
Senza trattamento la mortalità per Leishmaniosi viscerale è >90% e può sopraggiungere per complicanze infettive, emorragiche o decadimento progressivo delle condizioni generali.
Il trattamento di scelta in un paziente immunocompetente è costituito da Amfotericina B liposomiale (3 mg/kg/die ev per 5 giorni consecutivi, da ripetere 14a e 21° giornata). In alternativa può essere utilizzata la meltifosina o la paromomicina e, come seconda scelta alla luce dell’elevata tossicità, la terapia antimoniale pentavalente.
Quali sono i parametri utili per verificare la risposta al trattamento?
I dati clinico-laboratoristici sono sufficienti per valutare l’efficacia della terapia: l’apiressia viene raggiunta in meno di una settimana, dopo circa 10 giorni è apprezzabile una iniziale riduzione dell’epato-splenomegalia, che si risolverà in 3-6 mesi. La leucopenia e la trombocitopenia si correggono entro 30 giorni, mentre l’anemia può impiegare più tempo (fino a 6-12 mesi). Progressivamente migliora l’appetito e viene recuperato il peso corporeo.
La recidiva dovuta a un trattamento inefficace (ricaduta di segni/sintomi, associati a una conferma parassitologica) può verificarsi anche più di un anno dopo il termine del trattamento, ma generalmente si manifesta entro sei mesi.
La sierologia può rimanere positiva per oltre un anno dopo il termine della terapia, quindi non dovrebbe essere utilizzata nel follow up.
Il nostro paziente….
….viene ricoverato presso il reparto di Malattie Infettive dove viene praticata terapia con Amfotericina B liposomiale, come da protocollo. Nei 2 mesi successivi si assiste a scomparsa delle citopenie, negativizzazione degli indici di flogosi e riduzione dell’iper-gammaglobulinemia. Clinicamente non sono più rilevabili linfo-adenomegalie e si assiste a progressivo aumento ponderale; all’ecografia addome di controllo a distanza di un anno si documenta risoluzione della splenomegalia. Nei 2 anni successivi gli esami ematici trimestrali non mostrano anomalie di rilievo.
Diagnosis and Treatment of Leishmaniasis: Clinical Practice Guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH) (2016).
http://cid.oxfordjournals.org/content/early/2016/11/03/cid.ciw6 70.full.pdf+html (Accessed on November 16, 2016).
https://www.epicentro.iss.it/leishmaniosi/epidemiologia