

Giovanni Pomponio, Alessia Ferrarini
Dipartimento di Scienze cliniche e molecolari, Sezione Clinica medica
Facoltà di Medicina e Chirurgia, Università Politecnica delle Marche
Scenario clinico e specifica del setting di ricovero
Uomo di 81 anni presenta febbre fino a 38,5°C da 3 settimane associata a brividi scuotenti in assenza di altra sintomatologia d’organo. Il medico curante tentava, senza beneficio, una terapia antibiotica con ciprofloxacina, che veniva dunque sospesa tre giorni prima della nostra osservazione. Dall’anamnesi emergono i seguenti elementi: sostituzione valvolare aortica con protesi meccanica sei mesi prima e attualmente in terapia anticoagulante con warfarin; recente ictus con residua emiparesi destra; diabete mellito tipo II.
Giunge in un PS di un ospedale periferico dove vengono eseguiti:
- all’esame obiettivo: TC 38.5 °C, toni cardiaci tachicardici con soffio sistolico associato a rumore metallico udibili su tutti i focolai, tachipnoico, al torace murmure vescicolare normotrasmesso senza rumori patologici aggiunti, non organomegalie addominali, nella norma la restante obiettività
- Rx torace: negativo per addensamenti parenchimali
- ecocardiografia transtoracica: negativa per vegetazioni
- esami ematici: rialzo degli indici biologici di flogosi e anemia microcitica, leucocitosi con neutrofilia, nella norma lo studio della funzionalità renale ed epatica.
Viene ricoverato nel reparto di medicina generale dello stesso ospedale (dotato di laboratorio analisi, cardiologia, radiologia, pneumologia e chirurgia generale). Il medico di reparto, raccolta accuratamente l’anamnesi ed effettuato un esame fisico completo, definisce così il problema:
Febbre di origine sconosciuta in paziente portatore di valvola meccanica con ecocardio transtoracico negativo per vegetazioni.
Sulla base dei dati raccolti ipotesi più probabili nel caso osservato sono:
- febbre di origine infettiva, in modo particolare quella di endocardite su protesi valvolare, alla luce del recente intervento;
- malattia infiammatoria, vista l’età del paziente la polimialgia reumatica appare la più verosimile, benché l’assenza di sintomatologia tipica (dolore ai cingoli con caratteristiche infiammatorie) ne abbassi la probabilità;
- febbre neoplastica, il linfoma in primis e carcinomi.
Per verificare le ipotesi il medico richiede tre set di emocolture, l’urinocoltura, ed un’ecografia dell’addome che escludeva la presenza di linfoadenomegalie e di splenomegalia. Veniva richiesta una TAC addome e torace per escludere eventuali altri processi proliferativi.
Ragionando sul caso il medico si pone alcuni quesiti clinici.
Se un paziente risulta ad alto rischio di endocardite, la negatività dell’ecocardiogramma di superficie esclude la diagnosi? Come viene valutata la probabilità clinica di endocardite? Quali esami consentono di porre la diagnosi?
Per rispondere al quesito vengono prese in esame le ultime linee guida ESC (2015) per il trattamento dell’endocardite infettiva, prodotte dalla Società europea di Cardiologia, facilmente reperibili sul web.
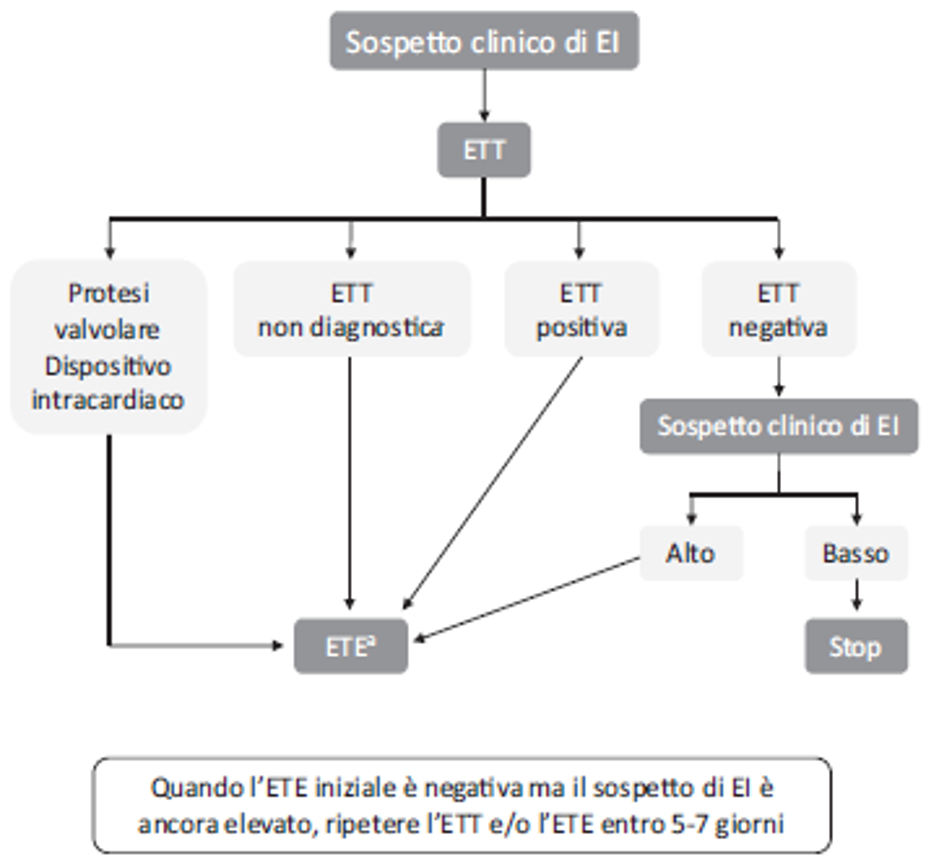
L’endocardite su valvola protesica rappresenta il 10-30% di tutti i casi di endocardite. Secondo le linee guida (Figura 1), posto il sospetto elevato di endocardite, in caso di portatore di valvola protesica risulta imperativo eseguire un’ecocardio transesofageo. Dunque il valore predittivo negativo di un ecocardio di superficie risulta essere basso in un contesto di elevata probabilità clinica. Nell’algoritmo diagnostico suggerito nelle stesse linee guida vengono forniti criteri maggiori e minori che si basano su reperti clinici, ecocardiografici e biologici, nonché sui risultati delle emocolture e dei test sierologici (criteri di Duke modificati). Questi consentono combinati tra loro di porre diagnosi clinica di endocardite, benché la sensibilità risulti minore nel contesto di una valvola protesica.
Il paziente veniva così sottoposto a un ecocardio transesofageo. Dall’esame emergeva la presenza di vegetazioni sulla valvola aortica protesica. Nel frattempo in due delle emocolture raccolte all’ingresso veniva isolato uno Staphylococcus aureus.
Secondo i criteri suggeriti, il paziente dunque è portatore di due criteri maggiori per la diagnosi di endocardite. Alla luce delle precedenti considerazioni viene posta diagnosi di endocardite infettiva precoce (ovvero a meno di 12 mesi dall’intervento chirurgico) su valvola protesica da Staphylococcus aureus.
Il germe isolato risulta essere uno dei principali responsabili nelle endocarditi che insorgono su valvola protesica, in particolar modo nelle endocarditi precoci. Questo comporta un rischio di mortalità elevato, determinando spesso la necessità di intervento di sostituzione valvolare. Veniva avviata terapia antibiotica endovenosa con Gentamicina 3 mg/kg/die in monodose e Vancomicina 30 mg/kg/die in 2 dosi come da linee guida, in attesa dell’antibiogramma. Inoltre ad oggi è pratica comune (benché supportato da bassi livelli di evidenza) associare Rifampicina 900-1200 mg e.v. o per os dopo 3-5 giorni dall’avvio della terapia antibiotica.
Impostata la terapia antibiotica il medico si trova davanti ad un’ulteriore difficolta nella gestione terapeutica del paziente. Infatti dalla sostituzione valvolare il paziente è in terapia anticoagulante con warfarin. Poiché è noto che la complicanza più frequente dell’endocardite infettiva è rappresentata dall’evento embolico, il paziente in terapia anticoagulante potrebbe risultare di conseguenza a più alto rischio di emorragia cerebrale su eventuali lesioni ischemiche emboliche.
Il medico si chiede dunque:
In un paziente con aumentato rischio emorragico per la presenza di endocardite infettiva e elevato rischio trombotico per la presenza di valvola meccanica è indicato mantenere la terapia anticoagulante?
Vengono ancora una volta prese in esame le linee guida ESC, dove vi sono solo raccomandazioni con bassi livelli di evidenza in merito alla gestione della terapia anticoagulante. Da una rapida revisione della letteratura emerge che il rischio di eventi embolici appare maggiore rispetto al rischio di evento emorragico. L’utilizzo della terapia anticoagulante è associata ad un minor rischio tromboembolico. Inoltre, per quanto riguarda la scelta dell’eventuale terapia anticoagulante vi è da chiarire quale terapia risulta preferibile tra terapia anticoagulante orale vs eparina a basso peso molecolare. La raccomandazione riportata nella linea guida ESC è: “nei pazienti con EI da Staphylococcus Aureus, in assenza di ictus, deve essere presa in considerazione la sostituzione della terapia anticoagulante orale con eparina non frazionata o a basso peso molecolare qualora venga valutata la possibilità di procedere al trattamento chirurgico”.
Il medico si trova di fronte ad una situazione in cui non vi sono chiare indicazioni. Viene dunque presa la decisione di non interrompere la terapia anticoagulate. Il paziente viene informato dell’aumentato rischio di ictus emorragico e il consenso informato alla prosecuzione della terapia anticoagulante viene registrato sul diario clinico. Viene proposta al paziente quindi la possibilità di sostituire la terapia orale con eparina a basso peso a dosi anticoagulanti, in vista dell’eventualità di intervenire chirurgicamente.
In un paziente con endocardite infettiva su valvola meccanica quali sono i criteri che predicono la necessità di intervento chirurgico?
Prendendo sempre come riferimento le Linee guida ESC 2015, qui è riportata una mortalità intraospedaliera per endocardite su valvola protesica estremamente elevata pari al 20-40%. Nelle linee guida ESC vengono riportate le indicazioni (Tabella 1) e le raccomandazioni alla chirurgia e il timing chirurgico per i pazienti considerati ad alto rischio, nonché una lista di fattori che classificano il paziente come ad alto rischio (Tabella 2). Nonostante ciò viene precisato che l’identificazione dei pazienti da candidare a trattamento chirurgico e il timing deve essere effettuata, caso per caso, dall’equipe multidisciplinare di specialisti. L’età avanzata non è considerata una controindicazione al trattamento chirurgico.
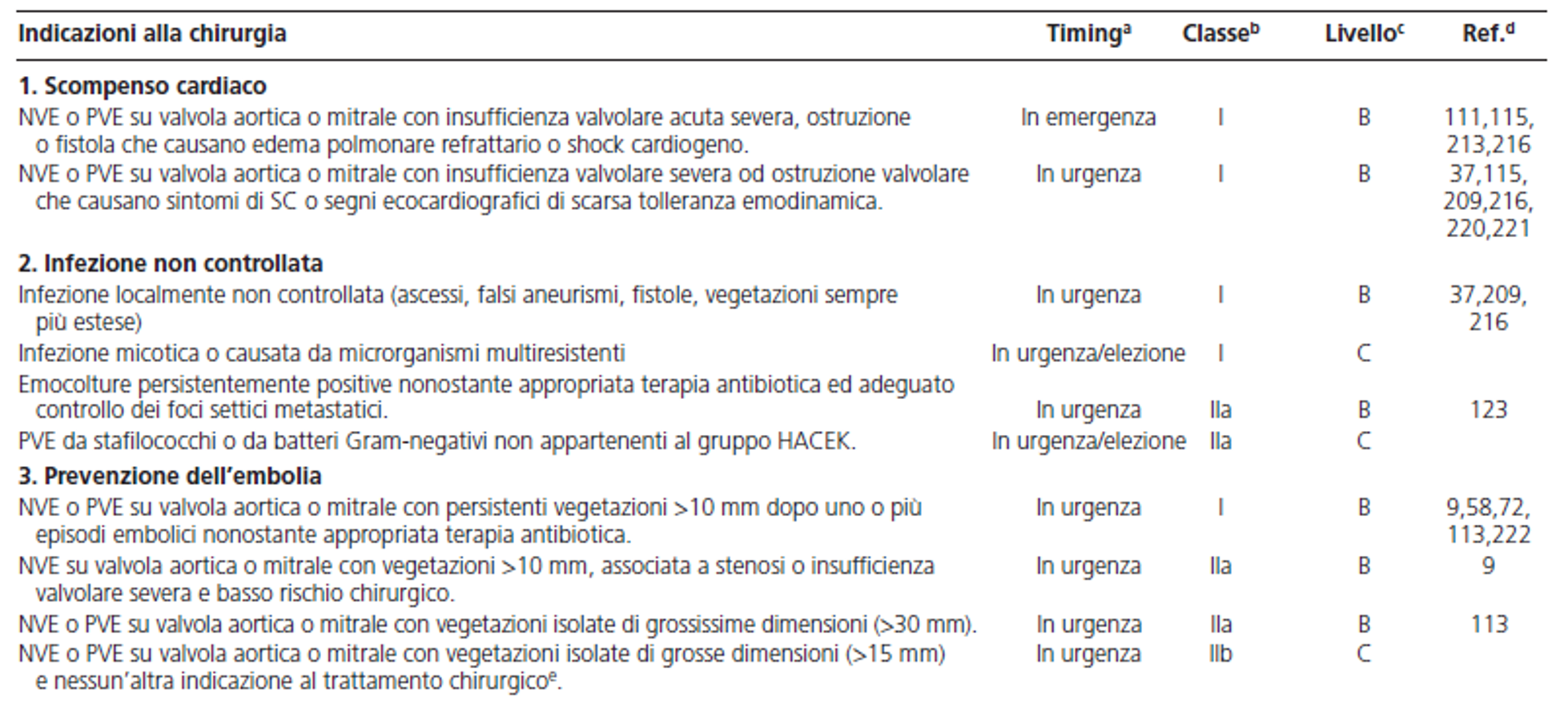
(endocardite su valvola nativa o valvola protesica). Linee Guida ESC 2015

Linee guida ESC 2015
Nel nostro caso il paziente risulta portatore di molteplici fattori predittivi di outcome sfavorevoli, in modo particolare: età avanzata, EI su valvola protesica, diabete mellito, recente ictus con residua emiparesi, e in modo particolare infezione da Staphylococcus aureus. Il paziente risulta dunque ad alto rischio e quindi candidabile ad un approccio chirurgico in regime di elezione/urgenza.
Il medico si pone infine un quesito gestionale.
Il medico si trova a valutare quale possa essere il setting assistenziale più appropriato ad un paziente anziano con endocardite infettiva su valvola protesica, emodinamicamente stabile, attualmente ricoverato in un reparto ordinario di un ospedale periferico
La opzioni a disposizione sono:
- trasferimento del paziente in unità di terapia intensiva
- trasferimento del paziente in un ospedale dotato di cardiochirurgia
- gestione del caso nel presidio ospedaliero periferico stesso
- trasferimento alle cure intermedie o al domicilio per completare la terapia antibiotica ed eventuale passaggio a terapia antibiotica orale.
Il trattamento in un reparto di medicina interna di un ospedale periferico rispetto al trasferimento in un reparto di un ospedale dotato di cardiochirurgia garantisce gli stessi esiti di salute? quando è necessario il trasferimento in un reparto di terapia intensiva? quali sono i criteri per un trasferimento sicuro in un reparto di cure intermedie? quali sono i criteri per la domiciliazione?
Le linee guida ESC raccomandano che il paziente venga valutato e gestito, almeno in fase iniziale, in un centro ospedaliero dotato di cardiochirurgia e rianimazione visto il maggior rischio di sviluppo di complicanze durante la fase acuta di infezione (0-2 settimane). Vengono inoltre specificate all’interno delle stesse linee guida le caratteristiche che definiscono il centro di riferimento. Solo successivamente in fase di stabilizzazione potrà essere valutata l’opportunità di proseguire la terapia antibiotica in regime ambulatoriale, rimandando dunque il paziente a domicilio.
Non vi sono specifici criteri per quanto riguarda le unità di terapia intensiva o presidi di lungo degenza/cure intermedie.
Tuttavia in caso di stabilità clinica dopo 15 giorni di trattamento, con paziente asintomatico e senza alterazioni strutturali o funzionali della sua protesi valvolare, può essere preso in considerazione il trasferimento in reparto di cure intermedie.
Da ultimo, come riportato in un recente lavoro del NEMJ, in condizioni cliniche stabili, la prosecuzione con terapia antibiotica orale risultata essere non meno efficace rispetto alla terapia endovenosa e può quindi essere valutata, in accordo con i care givers, la prosecuzione domiciliare del trattamento.
Alla luce delle raccomandazioni il paziente veniva trasferito in un ospedale di terzo livello e veniva sottoposto a intervento cardiochirurgico di debridement radicale e impianto di una nuova valvola protesica.
Per approfondire
- 2015 ESC Guidelines for the management of infective endocarditis: The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC), European Heart Journal, Volume 36, Issue 44, 21 November 2015, Pages 3075–3128, https://doi.org/10.1093/eurheartj/ehv319
- Prosthetic valve endocarditis: what is the evidence for anticoagulant therapy? Intern Med J. 2011 Nov;41(11):795-7 https://www.ncbi.nlm.nih.gov/pubmed/?term=prosthetic+valve+endocarditis+yau
- Partial Oral versus Intravenous Antibiotic Treatment of Endocarditis. N Engl J Med. 2018 Aug 28 https://www.ncbi.nlm.nih.gov/pubmed/?term=Partial+Oral+versus+Intravenous+Antibiotic+Treatment+of+Endocarditi